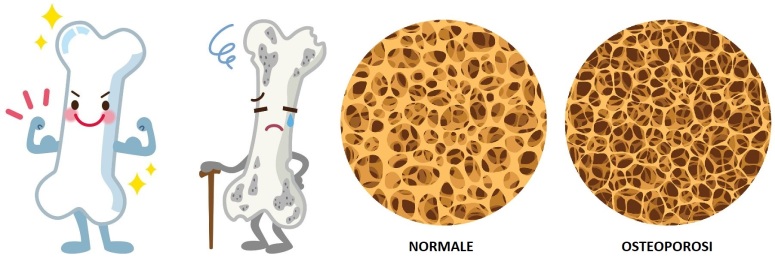
Per definizione, l’osteoporosi è una malattia metabolica dello scheletro ed è una delle principali osteopatie trattate dai MMG e medici specialisti in diversi settori. Tale condizione patologica è caratterizzata da un aumento della fragilità scheletrica e del rischio di fratture (consequenziali ad una riduzione della massa ossea mineralizzata).
FACCIAMO QUALCHE PASSO INDIETRO..
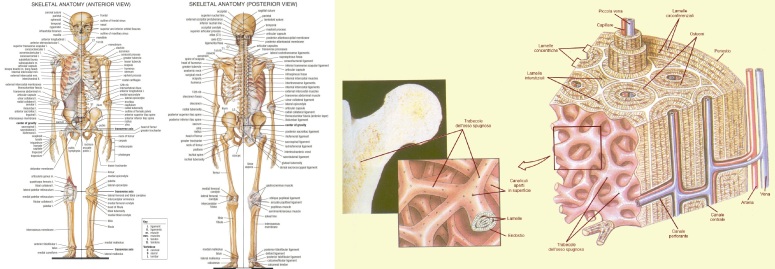
È risaputo che il tessuto osseo facente parte del nostro scheletro ha diverse importanti funzioni: sostegno del peso corporeo, protezione degli organi interni, ancoraggio dei muscoli con partecipazione ai movimenti, riserva di calcio/fosfati per il nostro organismo ed emopoiesi (formazione e maturazione degli elementi corpuscolati del sangue, ad es. GR, GB e piastrine).
Ciò che, però, è importante sapere, è che le ossa non sono strutture biologicamente “statiche”: il tessuto osseo è metabolicamente attivo e per tutta la durata della vita va incontro a processi di rimodellamento. Tale rimodellamento consiste in fasi di apposizione e fasi di demolizione (riassorbimento) ossea, mantenute in equilibrio sulla base delle necessità metaboliche dell’organismo.
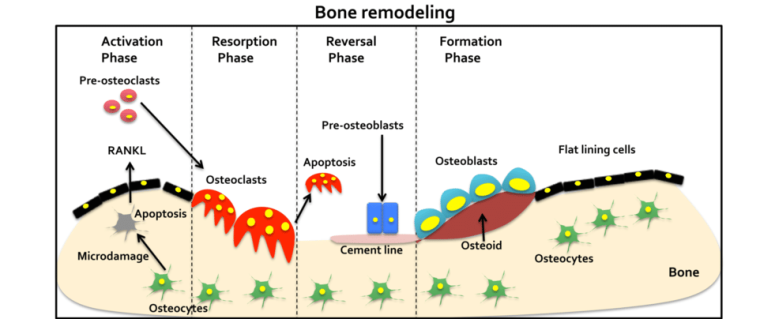
Quando, per svariate cause, questo equilibrio viene a mancare, si osserva l’insorgenza di quadri anatomo-clinici di differente gravità: l’osteoporosi è un esempio di questi.
STORIA
L’osteoporosi è conosciuta fin dai tempi più remoti: gli antichi medici, osservando le ossa dei cadaveri di soggetti anziani, si accorsero che nella maggior parte dei casi erano più leggere e porose delle normali ossa di un individuo adulto: le strutture interne apparivano particolarmente alterate con presenza di ampi spazi vuoti (da qui il termine osteoporosi).
La prima descrizione moderna di tale patologia risale al 1885, ma i primi veri studi si attestano soltanto verso la fine degli anni ’40.
Fino a una ventina d’anni fa l’osteoporosi non era considerata una patologia, ma solo una naturale ed inevitabile conseguenza dell’invecchiamento. Pertanto le fratture di femore/vertebre negli anziani erano reputate soltanto una fatalità che sfuggiva ad ogni possibilità di controllo.
Oggi, si è finalmente compreso come l’osso, pur andando incontro ad un processo di invecchiamento (come gli altri organi e tessuti del nostro corpo), non necessariamente deve arrivare a a quel grave impoverimento della sua componente minerale che lo fa diventare fragile e a rischio di frattura: è pertanto utile e necessario prevenire tale condizione. Si è compreso inoltre che la patologia non dipende soltanto da un processo di invecchiamento ma può essere dovuta anche ad altre eventuali condizioni che vanno opportunamente studiate e valutate in modo da effettuare una giusta diagnosi e pianificare un’adeguata terapia.
EPIDEMIOLOGIA
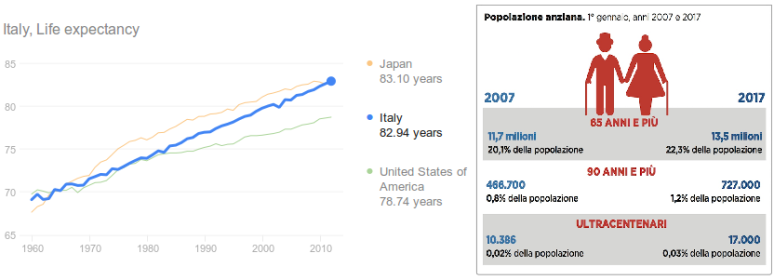
L’aumento progressivo dell’aspettativa di vita della popolazione mondiale (aumento della popolazione anziana) ha fatto sì che tale patologia, per le conseguenze cui può esporre, sia diventata una delle principali emergenze sociali del XXI secolo. In Europa circa il 30% delle donne in postmenopausa è affetto da osteoporosi e oltre il 40% di queste presenterà fratture osteoporotiche nel corso della sua vita. Le percentuali riguardo la mortalità e la morbilità in seguito a fratture da osteoporosi non sono certamente incoraggianti, allo stesso modo le ricadute sulla sanità pubblica in termini di costi (ospedalizzazione, invalidità).
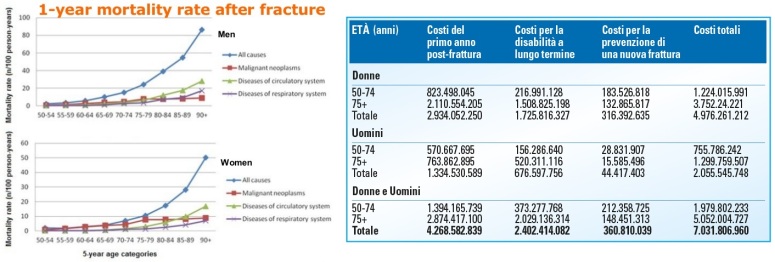
EZIOLOGIA E FISIOPATOLOGIA
Abbiamo precedentemente nominato la popolazione femminile in virtù del fatto che, oltre alla forma senile, la forma di osteoporosi con più alta incidenza è quella postmenopausale (osteoporosi primitive).
Esistono, ovviamente, diverse altre condizioni che possono portare a un quadro di osteoporosi (osteoporosi secondarie):
– Endocrinopatie (es. Cushing, ipogonadismo, deficit di GH, diabete, iperparatiroidismo, ipertiroidismo)
– Malattie ematologiche (es. mieloma multiplo)
– Malattie dell’apparato gastrointestinale (es. epatopatie, malassorbimento intestinale)
– Malattie reumatiche (es. AR, LES, spondilite anchilosante)
– Malattie renali (es. IRC)
– Malattie neurologiche (es. morbo di Parkinson, sclerosi multipla, distrofie muscolari)
– Malattie genetiche (es. Ehlers-Danlos, sindrome di Marfan, osteogenesi imperfetta)
– Altre malattie (es. AIDS, BPCO)
– Stati carenziali (es. calcio, vitamina D)
– Cause iatrogene (es. terapia cortisonica)
Dopo la maturità scheletrica, in entrambi i sessi (più precocemente nella donna), si assiste a una graduale perdita della massa ossea determinata da uno squilibrio del turnover tissutale: il riassorbimento inizia a prevalere sulla neoformazione.
Ciò che ci porta a definire le donne come principali soggetti a rischio è sicuramente il ruolo chiave degli ormoni steoridei anabolizzanti nella fisiopatologia dell’osteoporosi: la caduta degli estrogeni in menopausa, attraverso complessi meccanismi citochino-mediati (non ancora completamente noti), porta ad alcune modificazioni nella fisiologia ossea. Un esempio di tali modificazioni sono l’evidenza di un’aumentata osteoclastogenesi (osteoclasti= cellule che determinano il riassorbimento osseo) come anche l’alterata secrezione di PTH o aumento della sensibilità ossea a tale ormone (il PTH, in condizioni di ipocalcemia, aumenta la mobilizzazione di calcio dall’osso mediante azione indiretta sugli osteoclasti).
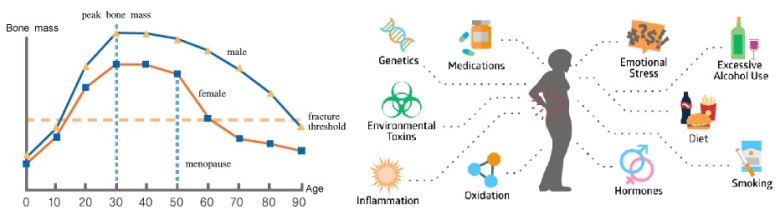
Per approfondire un quadro clinico di osteoporosi, quindi, bisogna tenere in considerazione molti aspetti che entrano a far parte di una complessa rete di cause e mai ragionare a compartimenti stagni.
Nel soggetto anziano, ad esempio, abbiamo una serie di problematiche connesse al metabolismo dell’osso: il ridotto assorbimento di calcio a livello intestinale, ridotta capacità del rene nell’idrossilare (attivare) la vitamina D, ridotta produzione di enzimi capaci di digerire il lattosio (e consequenziale riduzione dei latticini nella dieta con minore apporto di calcio), ridotta esposizione del soggetto ai raggi solari (ridotta quota di vitamina D attiva).
Bisogna quindi agire su ogni piccolo aspetto in modo da migliorare significativamente le condizioni del paziente e prevenire la patologia con annesse complicazioni.
ASPETTI CLINICI
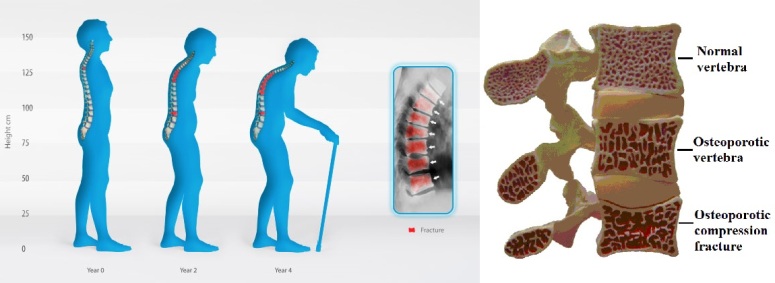
L’osteoporosi è una patologia che non arriva mai di colpo, a ciel sereno. Così come per l’ipertensione o l’ipercolesterolemia, l’osteoporosi è una malattia silenziosa che può progredire per anni fino alla diagnosi o alle complicanze (la frattura nel caso dell’osteoporosi, l’evento cardiovascolare nel caso dell’ipertensione/ipercolesterolemia).
Essendo di per sé una patologia asintomatica, spesso la diagnosi viene fatta su radiogrammi eseguiti per altri motivi o perché si ha comparsa di dolore dorsale e/o lombare subacuto (spesso dovuto a microfratture dei corpi vertebrali).
Il collasso vertebrale determina, nella maggior parte dei casi, un’ipercifosi dorsale molto marcata, associata ad iperlordosi lombare.
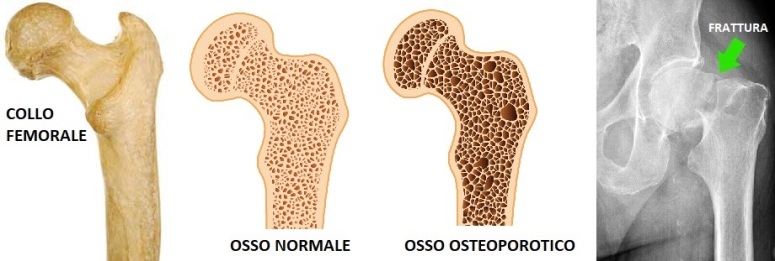
Oltre ai corpi vertebrali, i distretti ossei ulteriormente coinvolti dalle fratture da osteoporosi sono nella maggior parte dei casi femore/omero prossimale e radio/ulna distali.
DIAGNOSTICA STRUMENTALE
Diverse sono le tecniche diagnostiche che, insieme a un calcolo dei fattori di rischio, un’accurata anamnesi ed E.O. delle strutture scheletriche del paziente, ci permettono di identificare un quadro clinico di osteoporosi.
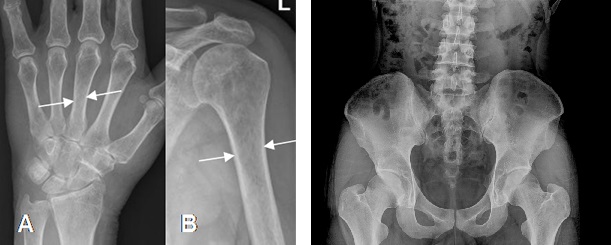
La radiografia standard (RX) è una metodica poco sensibile nelle fasi iniziali dell’osteoporosi: l’ipertrasparenza del tessuto trabecolare (sinonimo di ridotta densità minerale) diventa evidente soltanto quando si ha una perdita di oltre il 30% del contenuto minerale osseo.
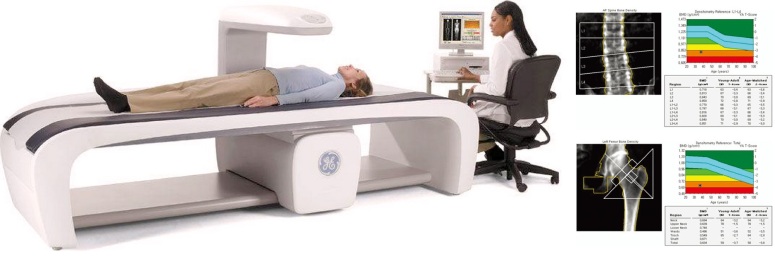
La mineralometria ossea computerizzata (MOC) con tecnica DEXA (Dual Energy X-ray Absorptiometry), è oggi considerata dall’OMS la tecnica più affidabile per identificare i soggetti con osteopenia/osteoporosi. Con tale indagine, è possibile effettuare misure densitometriche a livello del rachide lombare e del collo femorale (strutture con rapido turnover dell’osso trabecolare, ottimali per il monitoraggio della massa ossea).
La densità minerale viene identificata con la sigla BMD (Bone Mineral Density) ed è espressa in g/cm². Il valore della BMD del paziente viene confrontato col valore medio di soggetti adulti sani (di stessa età, sesso, altezza, etc) e in base alla deviazione standard (DS) da tale media (T-score) si interpreta il quadro clinico del paziente:
- BMD normale: T-score compreso tra +2,5 e -1,0 DS
- OSTEOPENIA: T-score compreso tra -1,0 e -2,5 DS
- OSTEOPOROSI: T-score inferiore a -2,5 DS
- OSTEOPOROSI CONCLAMATA: T-score inferiore a -2,5 DS e presenza di una o più fratture da fragilità
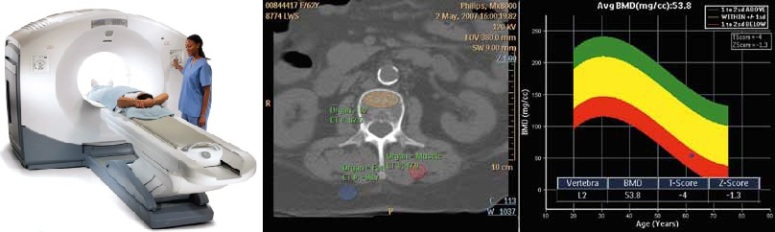
La tomografia computerizzata quantitativa (QTC) è un’altra indagine molto valida, soprattutto per la sua capacità di misurare la componente minerale ossea tenendo in considerazione la terza dimensione (spessore -> g/cm³). Nonostante abbia una maggiore precisione della DEXA, non è sempre indicata per via degli elevati costi e della maggiore radioesposizione.
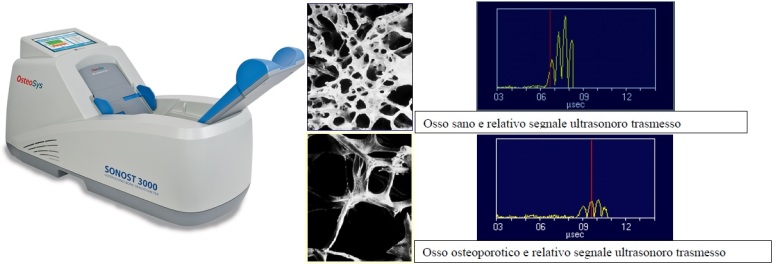
Un esame introdotto recentemente nel campo della diagnostica dell’osteoporosi è sicuramente l’osteosonografia. Ha bassissimo costo e invasività: si basa sulla capacità dell’onda ultrasonora di essere trasmessa attraverso un tessuto, con una velocità che dipende dalle caratteristiche del tessuto stesso. Nel caso dell’osso, lo stato di mineralizzazione della matrice influenza la velocità di trasmissione dell’onda, fornendo una precisa e accurata stima di predizione del rischio di frattura del paziente in base alla quantità di osso. È una metodica ancora in via di sviluppo, ma sta già dando risultati molto incoraggianti.
È importante, in riferimento a qualsiasi indagine strumentale trattata, sottolineare come la diagnosi clinica sia il risultato di una complessa valutazione di diagnostica differenziale: la diagnosi densitometrica sommata allo studio dei fattori di rischio (scheletrici ed extrascheletrici) aiutano il medico nel perfezionamento della diagnosi e nella pianificazione di una strategia terapeutica mirata e specifica per il singolo paziente.
DIAGNOSTICA DI LABORATORIO
Gli esami di laboratorio non hanno un ruolo chiave nella diagnostica delle osteoporosi primitive (senile, postmenopausale). VES, emocromo completo, protidemia, creatininemia e marcatori biochimici come la calcemia, fosforemia, calciuria, fosfatasi alcalina, calcitonina, paratormone, vitamina D e altri specifici, sono utilizzati prevalentemente per la diagnostica differenziale.
TERAPIA
Se fino a 20-30 anni fa la perdita di massa ossea senile/postmenopausale è stata considerata un processo irreversibile, da anni sono disponibili farmaci che permettono di inibire il riassorbimento osteoclastico, mentre la possibilità di stimolazione farmacologica della neoapposizione ossea rimane ancora dubbia.
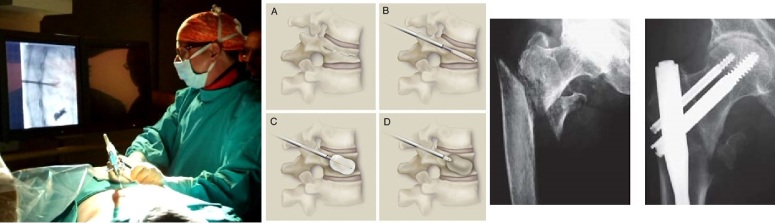
In pratica, l’osteoporosi può essere più efficacemente prevenuta che curata. Una terapia vera e propria è attuabile solo per quanto riguarda le fratture avvenute come complicanza della malattia (es. analgesici, busti, vertebroplastica/cifoplastica, trattamento chirurgico delle fratture di femore, artroprotesi).
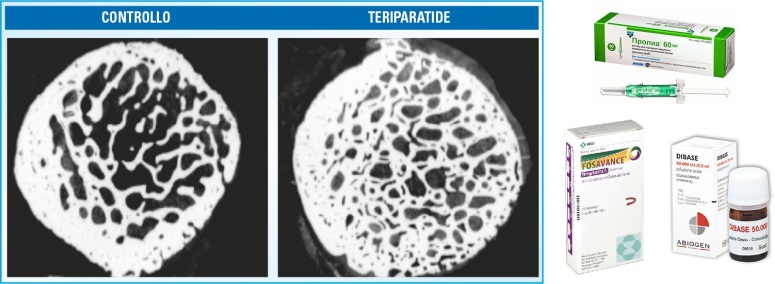
La terapia preventiva farmacologica si avvale di diversi farmaci:
– Steroidi gonadici: un esempio è la terapia sostitutiva nell’insufficienza ovarica con estro-progestinici. Il loro impiego non può essere protratto per più di 5-6 anni (aumentano il rischio di sviluppo di carcinomi dell’endometrio e della mammella)
– Calcitonina: diminuisce l’attività osteoclastica
– Difosfonati (es. Alendronato, Risedronato, Zolendronato): diminuiscono l’attività osteoclastica
– Vitamina D: viene utilizzata negli stati carenziali/insufficienza per migliorare l’assorbimento intestinale di calcio (spesso somministrata in associazione a quest’ultimo)
– Altri farmaci: modulatori selettivi del recettore estrogenico o SERMs (es. Raloxifene), frazione del PTH stimolante la neoformazione ossea (es. Teriparatide), anticorpi monoclonali con attività anti-osteoclastica (es. Denosumab), ranelato di stronzio
– Nuove prospettive terapeutiche: Odanacatib (inibitore selettivo della catepsina K, enzima chiave dell’attività osteoclastica; interrotto lo sviluppo clinico nel 2016 per aumentato rischio di ictus); anticorpi monoclonali neutralizzanti la sclerostina (inibitore fisiologico del sistema Wnt essenziale per la neoformazione di osso; es. Romosozumab)
Importantissimi sono anche gli interventi non farmacologici che possiamo effettuare per impedire/rallentare la comparsa dell’osteoporosi o per aiutare a ridurre il rischio di sviluppo di una frattura da fragilità:
– Alimentazione: regolare apporto di calcio, vitamina D e proteine.
– Attività fisica: è importante mantenere un minimo grado di attività fisica: in particolare, negli anziani, può contribuire a ridurre il rischio di cadute migliorando la funzione muscolare. Più incerta appare l’utilità dell’attività fisica nella prevenzione dell’osteoporosi.
– Interventi sul rischio di caduta: la disabilità motoria, disturbi dell’equilibrio, patologie neuromuscolari/neurodegenerative, disturbi cardiovascolari con perdita del controllo motorio, trattamenti farmacologici sono da tenere sotto controllo in un contesto di interventi multidisciplinari.

Per quanto riguarda i soggetti anziani, quindi, è altamente raccomandabile una strategia di prevenzione delle cadute che includa un adeguato apporto di vitamina D, esercizi fisici ed educazione sui rischi domestici.
– Mattia Nardolilli, Medicina e Chirurgia, Università degli studi “La Sapienza” di Roma (Policlinico Umberto I)

